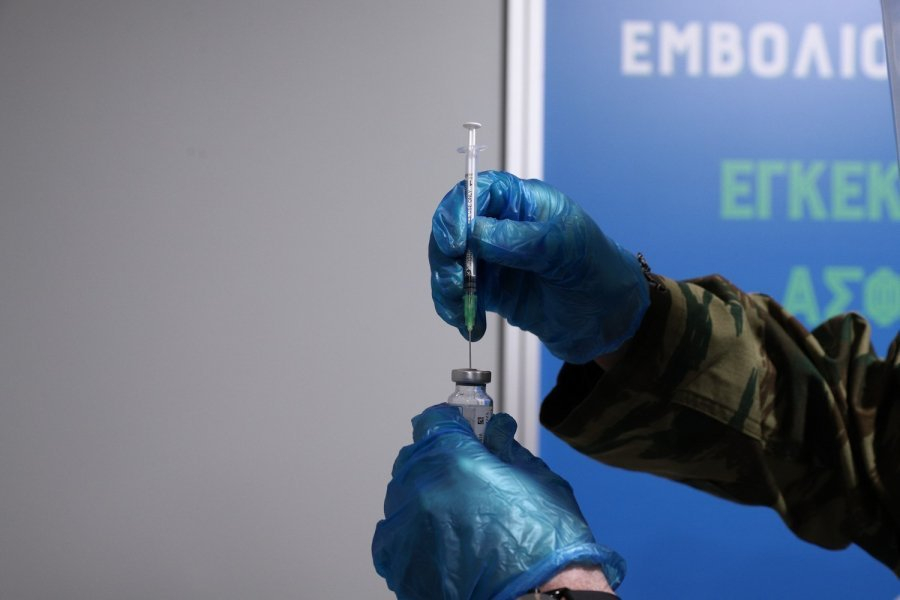
Σε παιδιά ηλικίας 5-11 ετών επεκτείνουν τις κλινικές δοκιμές του εμβολίου Pfizer/BioNTech και Moderna σύμφωνα με δημοσίευμα της Daily Mail
Η κίνηση αυτή έρχεται, όπως αναφέρει η «Daily Mail», κατόπιν αιτήματος της Αμερικανικής Υπηρεσίας Τροφίμων και Φαρμάκων (FDA).
Πηγές ανέφεραν στους «The New York Times» ότι η παρότρυνση για τις κλινικές δοκιμές γίνεται για να βοηθήσει στον εντοπισμό περιπτώσεων σπάνιας καρδιακής φλεγμονής που έχουν συμβεί σε εμβολιασμένα άτομα κάτω των 30 ετών.
Όταν ξεκίνησαν οι μελέτες, η Pfizer και η Moderna, της οποίας πριν από λίγες ημέρες εγκρίθηκε το εμβόλιο για τους 12-17 ετών, κλήθηκαν να συμπεριλάβουν 3.000 παιδιά, ηλικίας από 5 έως 11 ετών. Ωστόσο, οι εταιρείες καλούνται τώρα να διπλασιάσουν τον αριθμό των συμμετεχόντων.
Υπενθυμίζεται οτι σύμφωνα με ανακοίνωση την Πρόεδρο της Εθνικής Επιτροπής Εμβολιασμού γ Μαρία Θεοδωρίδου με βάση τα επιδημιολογικά δεδομένα της χώρας μας και την αυξανόμενη διασπορά της μετάλλαξης Δέλτα, λαμβάνοντας υπόψιν τη διαθεσιμότητα εμβολίων, η Επιτροπή γνωμοδοτεί θετικά για εμβολιασμό όλων των παιδιών 12 ως 15 ετών. Υπό τις παρούσες συνθήκες τα ωφέλη υπερτερούν. Ο εμβολιασμός είναι εθελοντικός και είναι απαραίτητη η συγκατάθεση των γονέων».
Από την πλευρά του ο γγ Πρωτοβάθμιας Φροντίδας Υγείας, Μάριος Θεμιστοκλέους, ανέφερε: «Έχουμε ανοίξει την πλατφόρμα για κατ' οίκον. Έχει εμβολιαστεί 410 πολίτες. Εδώ και περίπου 10 μέρες έχουμε ξεκινήσει κινητά συνεργεία σε απομακρυσμένες περιοχές και έχουμε εμβολιάσει 5000 άτομα. Η Επιτροπή έδωσε την έγκριση και την Παρασκευή θα ανοίξει η πλατφόρμα».
Παράλληλα οι διεθνείς οργανισμοί, FDA ενέκριναν με αδειοδότηση από τον Μάιο το εμβόλιο Pfizer ενώ πριν 3 μέρες ο EMA ενέκρινε και της Moderna και για παιδιά από 12 ως 17 ετών.
Αποποίηση ευθύνης
Ο ιστότοπος είναι μια πλήρως αυτοματοποιημένη υπηρεσία συνάθροισης, ταξινόμησης και ανάρτησης συνοπτικών ειδήσεων και νέων από άλλους ελληνικούς ειδησεογραφικούς ιστότοπους, μέσω της τεχνολογίας RSS. Δεν αναλαμβάνουμε καμία ευθύνη για την επάρκεια, ποιότητα, πληρότητα ή ακρίβεια των ειδήσεων και των νέων που δημοσιεύονται. Δείτε περισσότερα στο τμήμα "Αποποίηση Ευθύνης" των Ορων Χρήσης.
